Los bioingenieros han conseguido superar un obstáculo importante en el camino hacia la consecución de órganos de reemplazo imprimidos en 3D con una técnica avanzada para tejidos de bioimpresión. Esta innovación permite a los científicos crear redes vasculares exquisitamente enredadas que imitan los pasadizos naturales del cuerpo por donde fluyen la sangre, el aire, la linfa y otros fluidos vitales.
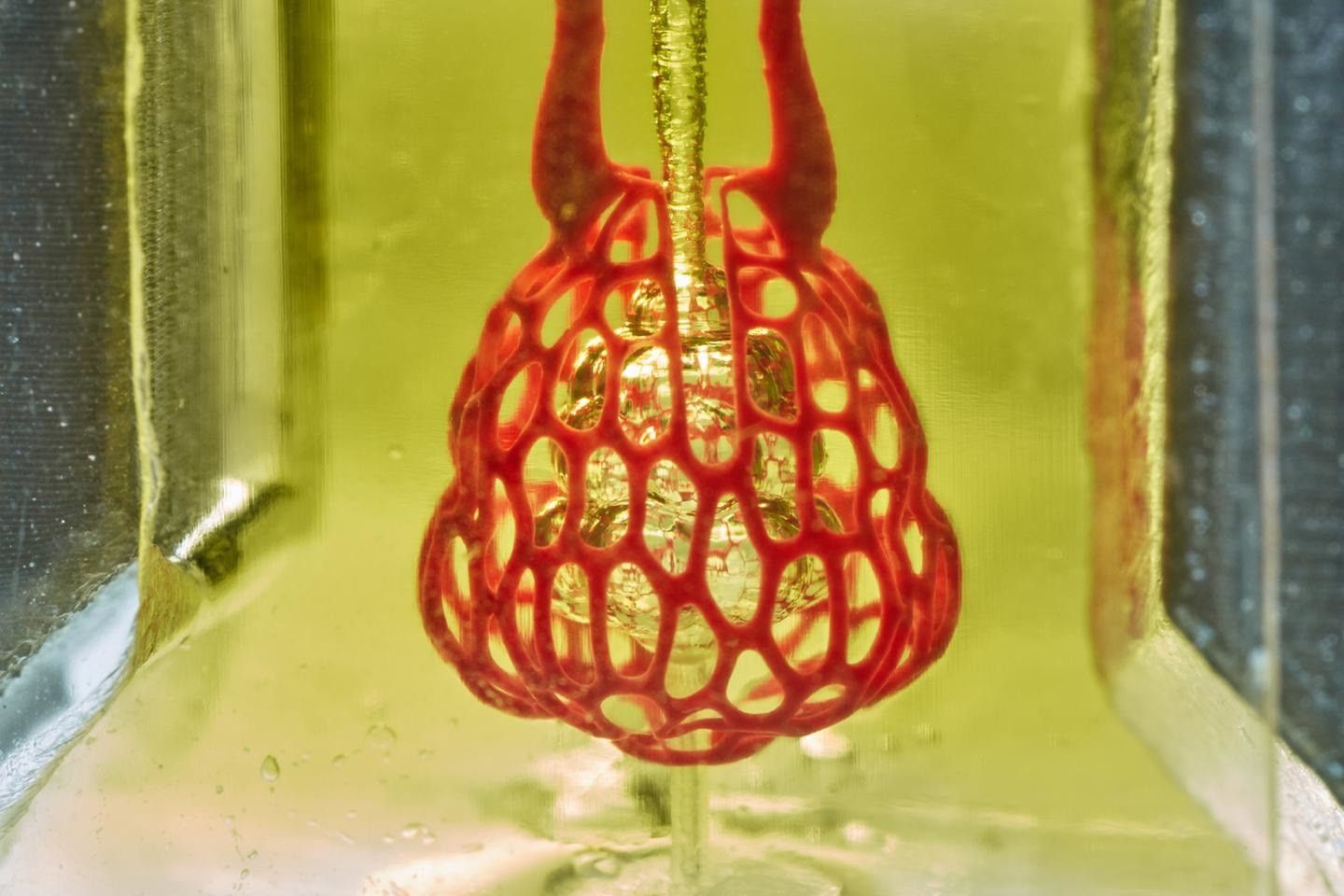
La investigación, aparece en la portada del número de esta semana de 'Science', incluye una prueba visualmente sorprendente: un modelo de hidrogel de un saco de aire que imita a los pulmones en el que las vías aéreas suministran oxígeno a los vasos sanguíneos circundantes.
El trabajo fue dirigido por los bioingenieros Jordan Miller, de Rice University y Kelly Stevens, de la University of Washington, e incluyó a 15 colaboradores de Rice, UW, Duke University, Rowan University y Nervous System, una firma de diseño en Somerville, Massachusetts.
"Uno de los mayores obstáculos para generar reemplazos de tejidos funcionales ha sido nuestra incapacidad para imprimir la compleja vasculatura que puede suministrar nutrientes a los tejidos densamente poblados --explica Miller, profesor asistente de bioingeniería en la Escuela de Ingeniería Brown de Rice--. Además, nuestros órganos en realidad contienen redes vasculares independientes, como las vías respiratorias y los vasos sanguíneos del pulmón o los conductos biliares y del hígado. Estas redes interpenetrantes están enredadas física y bioquímicamente, y la arquitectura en sí está íntimamente relacionada con el tejido. La nuestra es la primera tecnología de bioimpresión que aborda el desafío de la multivascularización de forma directa e integral".
Stevens, profesor asistente de bioingeniería en la Facultad de Ingeniería de la Universidad de Washington, profesor asistente de patología en la Escuela de Medicina de la Universidad de Washington e investigador en el Instituto de Medicina de Células Madre y Medicina Regenerativa de la Universidad de Wisconsin, añade que la multivascularización es importante porque la forma y la función a menudo van de la mano.
"La ingeniería de tejidos ha luchado con esto durante una generación. Con este trabajo, ahora podemos preguntarnos: '¿Podemos imprimir tejidos que permitan respirar como los tejidos sanos de nuestros cuerpos? ¿Se comportarán funcionalmente como esos tejidos?'. Esta es una pregunta importante, porque según lo bien que funcione un tejido de bioimpresión así será el éxito que tendrá como terapia".
El objetivo de la bioimpresión de órganos sanos y funcionales está impulsado por la necesidad de trasplantes de órganos. Solo en los Estados Unidos, más de 100.000 personas se encuentran en las listas de espera para trasplantes, y las que eventualmente reciben órganos de donantes se enfrentan toda una vida de medicamentos supresores del sistema inmunitario para prevenir el rechazo de órganos. La bioimpresión ha atraído un gran interés en la última década porque, en teoría, podría abordar ambos problemas al permitir que los médicos impriman órganos de reemplazo a partir de las propias células de un paciente. Se podría desplegar un suministro listo de órganos funcionales para tratar a millones de pacientes en todo el mundo.
De hecho, Miller asegura que se prevé "que la bioimpresión se convertirá en un componente importante de la medicina en las próximas dos décadas".
"El hígado es especialmente interesante porque realiza unas 500 funciones alucinantes, probablemente solo superadas por el cerebro --precisa Stevens--. Su complejidad significa que actualmente no hay una máquina o terapia que pueda reemplazar todas sus funciones cuando falla. Órganos humanos bioimpresos podrían hacerlo algún día".
Para abordar este desafío, el equipo creó una nueva tecnología de bioimpresión de código abierto denominada Aparato de Estereolitografía para Ingeniería de Tejidos (SLATE), que utiliza la fabricación aditiva para hacer hidrogeles suaves de una capa a la vez.
Las capas se imprimen a partir de una solución líquida de prehidrogel que se convierte en un sólido cuando se expone a la luz azul. Un proyector de procesamiento de luz digital ilumina desde abajo, mostrando cortes secuenciales en 2D de la estructura en alta resolución, con tamaños de píxeles de 10 a 50 micrones. Con cada capa solidificada, un brazo eleva el gel 3D en crecimiento lo suficiente para exponer el líquido a la siguiente imagen del proyector. La idea clave de Miller y Bagrat Grigoryan, un estudiante graduado de Rice y coautor principal del estudio, fue la adición de colorantes alimentarios que absorben la luz azul. Estos fotoabsorbentes limitan la solidificación a una capa muy fina. De esta manera, el sistema puede producir geles suaves, a base de agua y biocompatibles con la intrincada arquitectura interna en cuestión de minutos.
Las pruebas de la estructura que simula el pulmón mostraron que los tejidos eran lo suficientemente resistentes como para evitar estallar durante el flujo sanguíneo y la "respiración" pulsátil, una entrada y salida rítmicas de aire que simulaban las presiones y frecuencias de la respiración humana. Las pruebas encontraron que los glóbulos rojos pueden tomar oxígeno a medida que fluyen a través de una red de vasos sanguíneos que rodean el saco de aire que "respira". Este movimiento de oxígeno es similar al intercambio de gases que se produce en los sacos de aire alveolar del pulmón.
Para diseñar la estructura más complicada que imita Miller colaboró con las coautoras del estudio, Jessica Rosenkrantz y Jesse Louis-Rosenberg, cofundadoras del Nervous System.
Pruebas en ratones
En las pruebas de implantes terapéuticos para la enfermedad hepática, el equipo imprimió tejidos en 3D, los cargó con células hepáticas primarias y los implantó en ratones. Los tejidos tenían compartimentos separados para los vasos sanguíneos y las células hepáticas y se implantaron en ratones con lesión hepática crónica. Las pruebas mostraron que las células hepáticas sobrevivieron a la implantación.
Miller explica que el nuevo sistema de bioimpresión también puede producir características intravasculares, como válvulas bicúspides que permiten que el fluido fluya en una sola dirección. En los humanos, las válvulas intravasculares se encuentran en el corazón, las venas de las piernas y redes complementarias como el sistema linfático que no tienen bomba para impulsar el flujo.
Miller y Grigoryan están comercializando aspectos clave de la investigación a través de una empresa de nueva creación con sede en Houston llamada Volumetric, que está diseñando y fabricando bioimpresoras y biotintas.
Miller, un antiguo campeón de la impresión en 3D de código abierto, explica que todos los datos de origen de los experimentos en el estudio publicado de 'Science' están disponibles gratuitamente, al igual que todos los archivos imprimibles en 3D necesarios para construir el aparato de impresión de estereolitografía, y los archivos de diseño para imprimir cada uno de los hidrogeles utilizados en el estudio.
"Poner a disposición los archivos de diseño de hidrogel permitirá a otros explorar nuestros esfuerzos, incluso si utilizan alguna tecnología de impresión 3D futura que no existe hoy en día", confía Miller. Su laboratorio ya está utilizando el nuevo diseño y las técnicas de bioimpresión para explorar estructuras aún más complejas. "Solo estamos al comienzo de nuestra exploración de las arquitecturas que se encuentran en el cuerpo humano. Todavía tenemos mucho más que aprender", concluye.
Tienes que iniciar sesión para ver los comentarios