Si examinamos un cuerpo humano, encontramos tejidos muy diferentes en cuanto a su textura. Los huesos son muy duros, mientras que el cerebro y otros órganos son blandos. Esta propiedad (‘textura’) es esencial durante el desarrollo normal de un organismo, y su alteración está implicada en la aparición de patologías, fundamentalmente diversas formas de cáncer.
La textura de un tejido depende de varias propiedades, como el grado de densidad (‘compactación’) de las células, el tipo de proteínas que rodean a las mismas y la capacidad de las células para organizar el conjunto y endurecerlo, o mantenerlo blando. Para ello, las células disponen de ‘nano-motores’ que generan la fuerza necesaria para mantener o cambiar su forma y la de su entorno. Desde esta perspectiva, la formación de los tejidos es un proceso biofísico, aspecto que se suma a las tradicionales aproximaciones bioquímicas y genéticas, que han dominado la biología hasta ahora.
El nuevo campo de la mecánica celular (o mecanobiología) integra todos estos aspectos para desentrañar cómo funciona la maquinaria que controla estos procesos cuando ocurren normalmente, y trata de identificar elementos de desviación de la normalidad que causan cáncer y otras enfermedades. Gracias a estas líneas de investigación se pueden abrir nuevos estudios con aplicación en la asistencia médica.
El principal nano-motor celular que genera fuerza dentro de las células se denomina miosina II. Existen distintas variantes (musculares y no musculares), que tienen funciones esenciales en procesos básicos para la vida, desde el movimiento voluntario de los músculos hasta los movimientos involuntarios, como la respiración y el latido del corazón.
El trabajo previo del grupo del Dr. Miguel Vicente-Manzanares, Científico Titular del Centro de Investigación del Cáncer (CIC-IBMCC; centro mixto de la Universidad de Salamanca y del CSIC) había demostrado la existencia y estudiado la función de proteínas similares a las miosinas II musculares en todos los tejidos, incluso en neuronas y células sanguíneas. Esencialmente, todas las miosinas II, tanto las musculares como las no musculares, están compuestas por dos cadenas pesadas y cuatro ligeras.
La variante no muscular se encuentra en todas las células del organismo, y es el objeto de este estudio. Esta proteína controla todos los aspectos de la vida de la célula, generando la fuerza necesaria para que la célula tenga una forma concreta u otra, determinando su capacidad para moverse o dividirse, etc.
En el último número de la revista científica Current Biology, se describe un avance esencial para comprender los mecanismos que permiten a las células controlar su textura, y que es esencial para su capacidad de movimiento y especialización. El trabajo del grupo del Dr. Vicente-Manzanares concluye que una modificación concreta de una de las cadenas ligeras de la miosina II no muscular bloquea su función “a demanda”.
Este mecanismo había permanecido inédito hasta este estudio, pero es un avance esencial para comprender cómo las células se adaptan a su entorno y reciben señales del mismo para migrar, dividirse o cambiar su textura para formar un tejido. Este trabajo es pionero porque demuestra que la modificación descrita anteriormente impide que la miosina II forme los entramados que forman el “esqueleto celular” o citoesqueleto, que es necesario para que la célula tenga una forma concreta, se relacione con las células de su entorno inmediato y pueda moverse o dividirse.
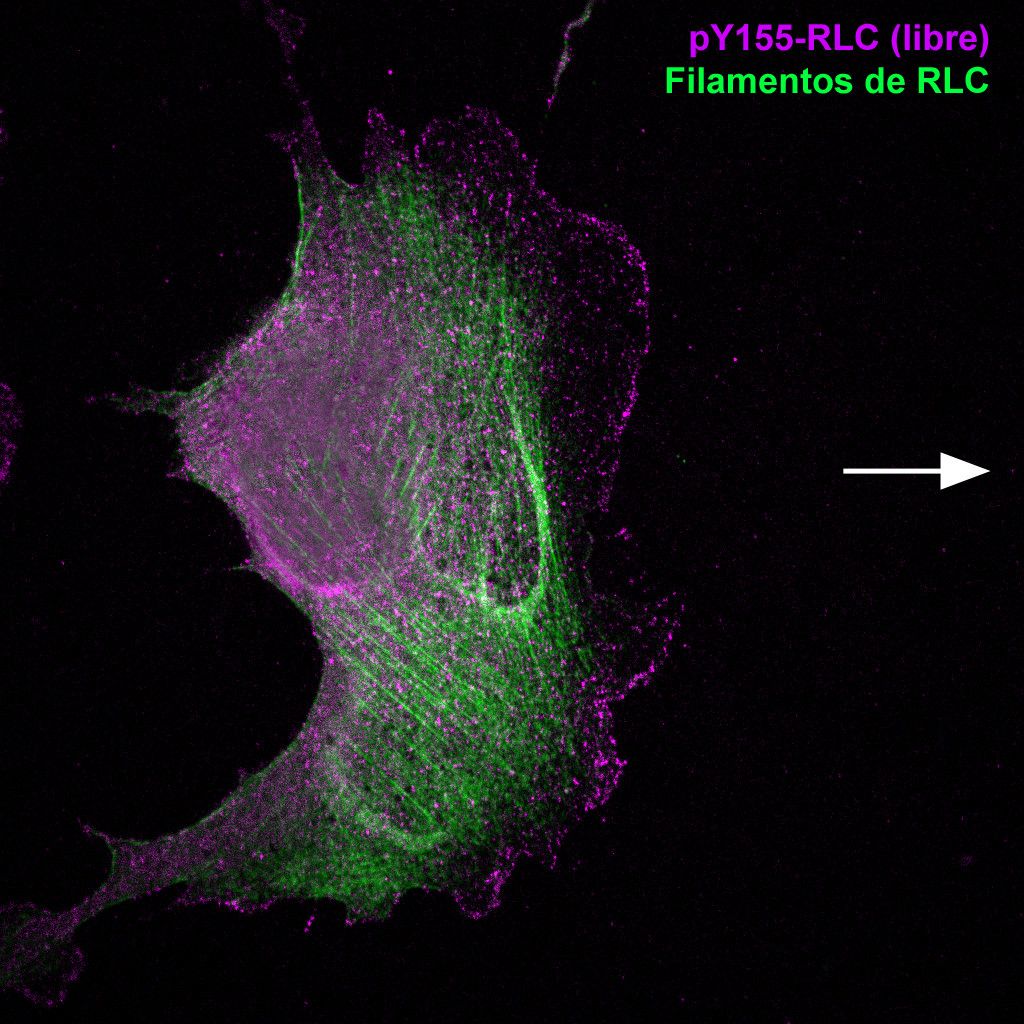
En concreto, la modificación descrita es una fosforilación en tirosina (Tyr155), que es una forma común de modificación de las proteínas para cambiar su función. En otras palabras, las proteínas fosforiladas pueden realizar funciones que no pueden hacer cuando no están fosforiladas. La fosforilación como proceso general fue objeto del Premio Nobel de Medicina concedido a Edmond Fischer y Edwin Krebs en 1992.
La fosforilación en tirosina 155 de la cadena ligera de la miosina II no muscular, objeto del estudio, impide que la miosina II forme entramados filamentosos (“esqueleto celular” o “citoesqueleto”) que son necesarios para generar fuerza. En este sentido, la miosina II ensamblada (es decir, no fosforilada en tirosina 155) actuaría como un albañil, que usa su fuerza para colocar y cementar los componentes de la célula, y así permitir su actividad normal.
La fosforilación en tirosina descrita en este artículo actúa como una “pausa forzosa para comer”, deteniendo el ensamblaje de la miosina, es decir, impidiendo el acceso del albañil a la obra.
Es importante reseñar que la fosforilación de otros componentes de la miosina II es esencial para su función y ensamblaje, lo que significa que esta fosforilación es parte de un complejo sistema de señales positivas y negativas que activan o inactivan la miosina II en función de las condiciones precisas de la célula y su entorno.
Este descubrimiento es básico para entender cómo las células controlan la cantidad exacta de fuerza que necesitan para realizar cada proceso y abre la puerta al estudio de la alteración de esta modificación en diversos tipos de cáncer caracterizados por la displasia, o pérdida de la forma celular, y la invasión y metástasis, que son procesos en los que la mecánica celular está alterada, haciendo que las células cancerosas, que no deberían migrar, se trasladen a otras regiones para formar tumores secundarios.
Este importante descubrimiento ha recibido apoyo financiero del Ministerio de Economía y Competitividad, la Junta de Castilla y León, la Asociación Española contra el Cáncer y las fundaciones Ramón Areces y BBVA.

Tienes que iniciar sesión para ver los comentarios